瀉血療法とは? いつ用いられる?

によって書かれ、確認されています。 医者 Maryel Alvarado Nieto
瀉血療法とは、患者の臨床状態を改善するために、大量の血液を採取する方法です。この技術は単に「瀉血(しゃけつ)」とも呼ばれ、古代には頻繁に行われていました。当時は、病気の効果的な治療というよりも、当時の人々の信仰に応えるために、さまざまな場面で使われていたようです。
実際、瀉血処置の多くは、利より害をもたらしました。そして科学が発達し、病態生理が解明されるにつれて、瀉血は次第に廃れていき、より病気の本質に迫った治療法に取って代わられたのです。しかし、今でも瀉血が有効な場合があります。
瀉血療法とは
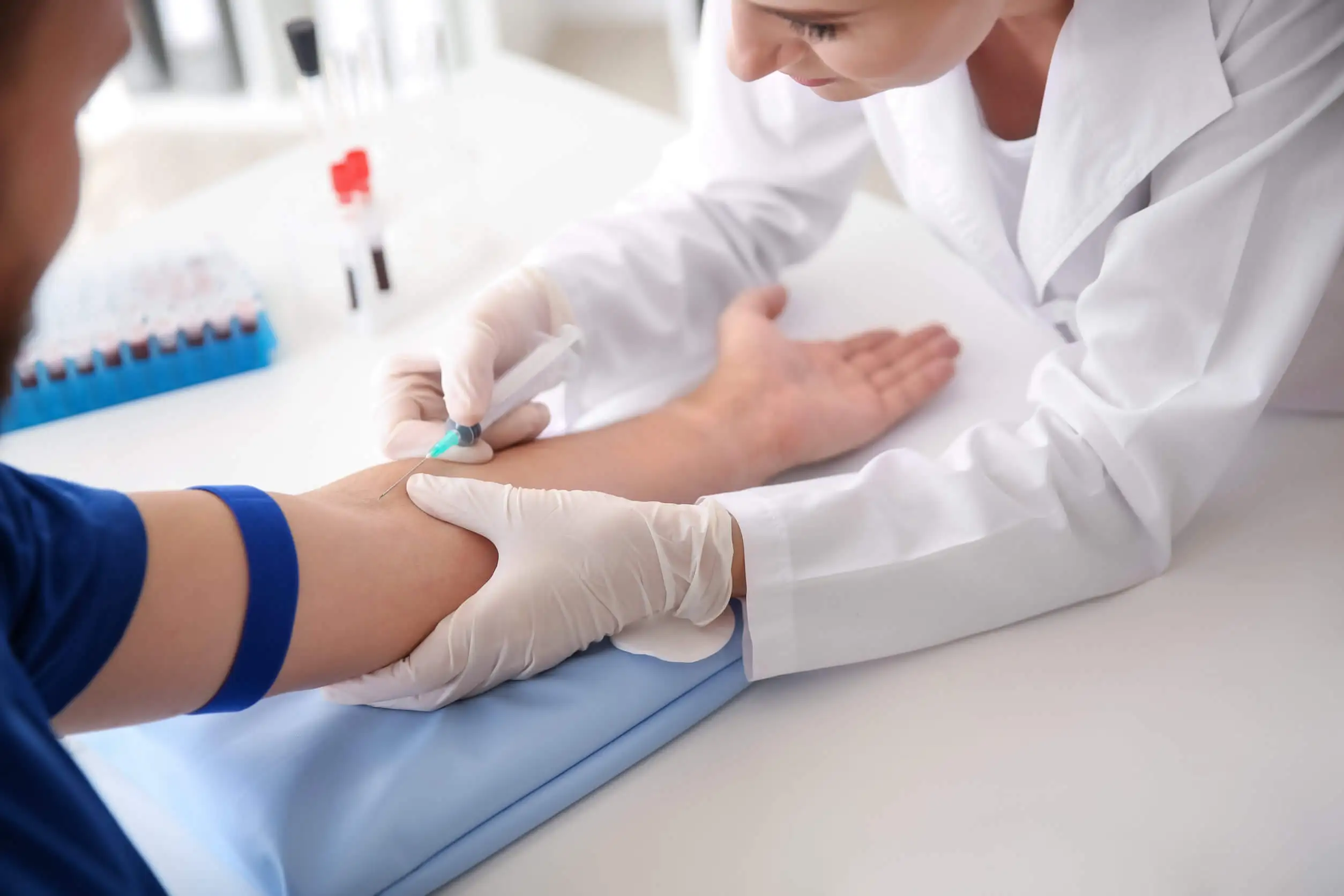
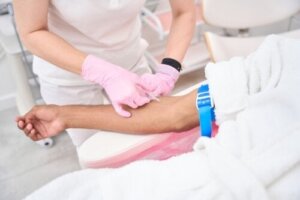
注射針と500mlの採血バッグがついた採血器具で末梢静脈(通常は前腕部)を穿刺し、採血します。
採血量は、出血の治療目的、患者の年齢や臨床状態によって異なります。採血秤を使用することで、リアルタイムに採血量を確認することができます。
施術時間は20~40分で、患者を半座位の姿勢に置きます。一方、採血バッグの位置は、重力によって血液が抽出されるように、処置中は腕の高さより下に設置します。
重要な考慮事項
瀉血療法を受ける患者は、処置の前にバイタルサインの記録と処置に関する適切な説明を受けておく必要があります。十分な水分補給と食事をしていることが重要です。処置後、患者は十分な水分を摂取し、急激に体を動かさないように注意します。
こちらもお読みください:本態性振戦:症状、原因、そして治療法
瀉血療法はどのような場合に行われる?
何世紀もの間、瀉血は様々な症状を治療するための一般的な処置でした。技術は初歩的なものでしたが、目的は、そこにあると信じられていた病気の原因を取り除くために十分な血液を採取することでした。
かつては多用されていたものの、現在では瀉血が治療法となるような臨床症状はほとんどありません。それでも、瀉血には依然として大きな反対意見があります。
遺伝性ヘモクロマトーシス
遺伝性ヘモクロマトーシス(HH)は、常染色体劣性遺伝する先天性疾患であり、代謝異常の中で最も多い遺伝性疾患です。
遺伝性ヘモクロマトーシスは、食事からの鉄の摂取量が増加し、鉄が体内に蓄積される疾患です。臨床症状は患者によって大きく異なり、症状が現れないケースもあります。
過剰な金属は体内の様々な臓器、特に肝臓、心臓、膵臓にダメージを与えるため、治療は鉄の沈着を徐々に減らし、結果として適切な鉄の値を維持することが基本になります。
このため、現在でも瀉血療法が有効な疾患の一つとなっています。実際、早期治療により肝硬変への進行を防ぎ、患者の生存率を向上させることができます。
初期の段階では、出血の頻度は1週間から2週間の間で、患者の状態や手技に対する耐性によって変化します。治療期間は6ヶ月から2年です。
正常値に達した後は、定期的に経過観察を行い、瀉血療法は時間を空けて行うべきと主張する維持療法ガイドラインに沿って瀉血が再び必要か評価します。
こちらもお読みください: 【脾臓の痛み】原因と治療
HH患者における瀉血の禁忌
すべての患者が瀉血に適しているわけではないので、他の治療法もあります。これらの治療法のいずれも実施できない場合、鉄キレート剤の使用に頼ることもあります。しかし、鉄キレート剤の使用ではあまり良い効果がこれまで認められていません。瀉血療法は、以下のような場合には禁忌とされています。
- 冠動脈疾患
- うっ血性心不全
- 貧血
- 高齢
晩発性皮膚ポルフィリン症の治療的瀉血療法について

また、体内の鉄の蓄積が関連する疾患として、晩発性ポルフィリン症があります。この疾患では、ポルフィリンを分解する肝臓の酵素が影響を受けるため、これらの分子が増加するのです。
主な臨床症状としては、皮膚の露出部に病変が出現し(光線過敏症)、さまざまな程度の肝機能障害があります。
このような患者では、鉄分値を下げることを目的に、瀉血を繰り返すことが第一選択治療となります。その理由は、過剰な金属が臓器障害を引き起こすことに加え、肝酵素の阻害を引き起こすからです。したがって、これらの沈着物を減らすことで、酵素が放出され、その結果、蓄積したポルフィリンが減少することになるのです。
遅発性皮膚ポルフィリン症の治療指針
瀉血による治療の適応は、定期的に血球計数的な指標をコントロールしながら、個別に判断する必要がある。一般的には、許容値に達するまで、時間をかけて抜血を行う。
しかし、再発の傾向があるため、医師は維持治療の必要性を評価する必要があります。このような患者では、抗マラリア薬と採血を併用することが一般的です。
アイゼンメンガー症候群
さまざまな先天性心疾患により、肺血管抵抗が増加し、肺高血圧症が出現します。最も重症の場合、アイゼンメンジャー症候群を発症します。
この症候群では、さまざまな病的メカニズムによって肺の毛細血管の血流が妨げられ、酸素交換が阻害され、低酸素血症の存在が引き金となえいます。
その結果、体はこの不足分を赤血球の増産で補おうとするのです。赤血球は体のさまざまな細胞に酸素を運ぶ役割を担っているからなのですが、赤血球が増えると血液中の造血成分(ヘマトクリット)の割合が増え、血液の粘度が高くなります。
この流動性の低下は、高粘度症候群と呼ばれる症状を引き起こし、治療的瀉血療法を行うことで緩和させることができます。
しかし、アイゼンメンジャー症候群の場合、ヘモクロマトーシスとは異なり、瀉血は決定的な治療法ではありません。また、その適用は鉄沈着物の減少につながるため、患者ごとに慎重に検討する必要があります。
慢性肺炎および治療的慢性肺疾患と瀉血療法
慢性肺疾患は、慢性的な低酸素状態により赤血球の産生が増加し、その結果、高粘度症候群を発症することがあります。
このため、瀉血は症状を治療し、患者の状態を改善するための選択肢の一つと考えることができます。しかし、ある研究では、長期間の追跡調査は行われておらず、この技術の有益性には疑問が残ります。
瀉血療法をめぐる論争
多くの国で血色素症患者から採取された血液が組織的に廃棄されていることについて、反省を求める声があります。これらの患者から得られた血液の質は、通常の血液バンクのドナーのそれと同等かそれ以上であることが示されており、血液を廃棄することは貴重な無駄であるという主張です。
同様に、採血された血液の使用を認めない唯一の正当な理由は、患者が瀉血療法を受けることによって健康上の利益を得ているため、本質的に利他的な献血にならないことだという意見もあります。
また、採血後、献血するかしないかを検討する必要があるという声もあります。この主張では、血液の提供によってもたらされる可能性を評価することが必要であることを強調しています。また、遺伝性ヘモクロマトーシスは遺伝性疾患であるため、輸血によって感染することはないことは明らかです。
引用された全ての情報源は、品質、信頼性、時代性、および妥当性を確保するために、私たちのチームによって綿密に審査されました。この記事の参考文献は、学術的または科学的に正確で信頼性があると考えられています。
- Domarus, A.; Farreras, P.; Rozman, C.; Cardelach, F.; Nicolás, J; Cervera, R.; Farreras Rozman. Medicina Interna; 19na Edición; Elsevier; 2020.
- Ortiz, I.; Paredes, J.; López, A.; Moreno, E.; Hemocromatosis: Etiopatogenia, Diagnóstico y Estrategia Terapéutica; Medicine: Programa de Formación Médica Continuada Acreditado; Elsevier; 19 (19): 1153 – 1561; 2012.
- Tapias, M.; Idrovo, V.; Hemocromatosis Hereditaria; Asociaciones Colombianas de Gastroenterología, Endoscopia Digestiva, Coloproctología y Hepatología; Revistra Colombiana de Gatroenterología; 21 (4): 278 – 285; 2006.
- Adams, P.; Altes, A.; Brissot, P.; Butzeck; B.; Cabantchik, I.; Cançado, R.; Distante, S.; Evans, P.; Evans, R.; Ganz, T.; Girelli, D.; Hultcrantz, R.; McLaren, G.; Marris, B.; Milman, N.; Nemeth, E.; Nielsen, P.; Pineau, B.; Piperno, A.; Porto, G.; Prince, D.; Ryan, J.; Sanchez, M.; Santos, P.; Swinkles, D.; Teixera, E.; Toska, K.; Vanclooster, A.; White, D.; Recomendaciones Terapéuticas en Hemocromatosis con el Genotipo Homocigoto HFE p.Cys282Tyr (C282Y/C282Y); Haemochromatosis International; 2018.
- Hernández, A.; Hemocromatosis, Donación de Sangre y Altruismo; Bioètica & Debat: Tribuna Abierta del Institut Borja de Bioètica; 42: 8 – 11; 2005.
- Romero, M.; La Hemocromatosis como Polémica Fuente de Donación de Sangre; Medicina Clínica; 128 (13): 515; 2007.
- Sandoval, J.; Síndrome de Eisenmenger: Avances en la Patobiología y Tratamiento; Archivos de Cardiología de México; 72 (Suplemento 1): S207 – S211; 2002.
- Toloza, L.; Flebotomía Terapéutica en Pacientes con Neumopatía Crónica: Estudio Observacional de un Grupo de Pacientes Atendidos en un Banco de Sangre a 2600 m.s.n.m.; Trabajo de Grado; Universidad Nacional de Colombia; Facultad de Medicina; Departamento de Medicina Interna; 2015.
- Calderón, J.; Sandoval, J.; Beltrán, M.; Hipertensión Pulmonar y Cardiopatía Congénita Asociado a Síndrome de Eisenmenger; Archivos de Cardiología de México; 85 (1): 32 – 49; 2015.
- Góngora, R.; La Sangre en la Historia de la Humanidad; Revista Biomédica; 16: 281 – 288; 2005.
- Parker, D.; Deel, P.; Arner, S.; Los Detalles de la Flebotomía Terapéutica; Nursing, 22 (10): 40 – 41; 2002.
このテキストは情報提供のみを目的としており、専門家との相談を代替するものではありません。疑問がある場合は、専門家に相談してください。